Βιβλιογραφική αναφορά: PERGOSAFE Επικαλυμμένα με λεπτό υμένιο δισκία για άλογα (2023)
Είδη ζώων
Άλογα (μη προοριζόμενα για ανθρώπινη κατανάλωση).
Θεραπευτικές ενδείξεις για κάθε είδος ζώου
Συμπτωματική θεραπεία των κλινικών συμπτωμάτων που συσχετίζονται με τη δυσλειτουργία του διάμεσου λοβού της υπόφυσης (PPID) (νόσος του Cushing των ιπποειδών).
Οδοί χορήγησης και δοσολογία
Από στόματος χρήση, μία φορά ημερησίως.
Για τη διευκόλυνση της χορήγησης, η απαιτούμενη ημερήσια δόση θα πρέπει να τοποθετείται σε μικρή ποσότητα νερού ή/και να αναμειγνύεται με μελάσα ή άλλο γλυκαντικό και να αναδεύεται μέχρι να διαλυθεί. Σε αυτήν την περίπτωση, τα διαλυμένα δισκία πρέπει να χορηγούνται με σύριγγα. Ολόκληρη η ποσότητα πρέπει να χορηγηθεί αμέσως. Τα δισκία δεν πρέπει να θρυμματίζονται, βλ. κεφάλαιο 3.5.
Δόση έναρξης
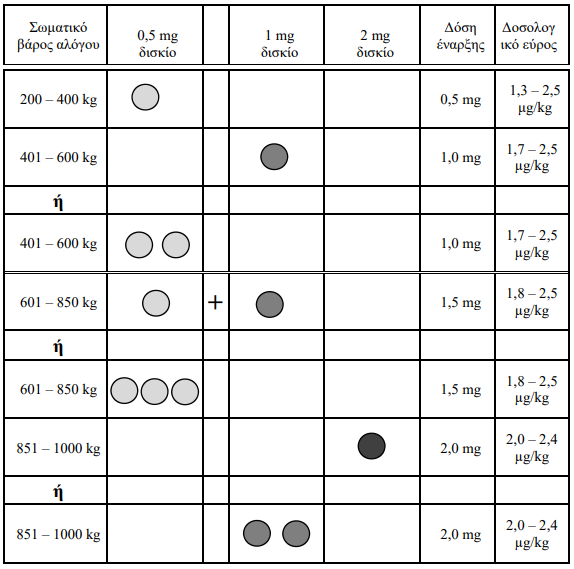
Η δόση έναρξης είναι περίπου 2 μg περγολίδης/kg (δοσολογικό εύρος: 1,3 έως 2,5 µg/kg· βλ. πίνακα παρακάτω). Η δόση συντήρησης θα πρέπει στη συνέχεια να τιτλοποιείται σύμφωνα με την ατομική ανταπόκριση, όπως αυτή καθορίζεται από την παρακολούθηση (βλ. παρακάτω), με αποτέλεσμα μια μέση δόση συντήρησης 2 µg περγολίδης/kg σωματικού βάρους με δοσολογικό εύρος από 0,6 έως 10 µg περγολίδης/kg σωματικού βάρους.
Οι δόσεις έναρξης συνιστώνται ως εξής:
Δόση συντήρησης
Η δια βίου θεραπεία είναι αναμενόμενη για αυτήν τη νόσο. Τα περισσότερα άλογα ανταποκρίνονται στη θεραπεία και σταθεροποιούνται σε μια μέση δόση 2 µg περγολίδης/kg σωματικού βάρους. Κλινική βελτίωση με την περγολίδη αναμένεται εντός 6 με 12 εβδομάδες. Τα άλογα μπορεί να ανταποκριθούν κλινικά σε χαμηλότερες ή διαφορετικές δόσεις· συνιστάται επομένως η τιτλοποίηση στη χαμηλότερη αποτελεσματική δόση ανά άτομο με βάση την ανταπόκριση στη θεραπεία, είτε πρόκειται για αποτελεσματικότητα είτε για συμπτώματα μη ανεκτικότητας. Ορισμένα άλογα μπορεί να χρειαστούν δόσεις έως και 10 μg περγολίδης/kg σωματικού βάρους ημερησίως. Σε αυτές τις σπάνιες περιπτώσεις, συνιστάται η κατάλληλη πρόσθετη παρακολούθηση.
Μετά από την αρχική διάγνωση, επαναλάβετε τις ενδοκρινολογικές εξετάσεις για την τιτλοποίηση της δόσης και την παρακολούθηση της θεραπείας ανά διαστήματα 4 έως 6 εβδομάδων έως ότου επέλθει σταθεροποίηση ή βελτίωση των κλινικών συμπτωμάτων ή/και των διαγνωστικών εξετάσεων.
Εάν τα κλινικά συμπτώματα ή οι διαγνωστικές εξετάσεις δεν έχουν ακόμη βελτιωθεί στο πρώτο διάστημα 4 έως 6 εβδομάδων, η συνολική ημερήσια δόση μπορεί να αυξηθεί κατά 0,50 mg. Σε περίπτωση που τα κλινικά συμπτώματα έχουν βελτιωθεί αλλά δεν έχουν ακόμη ομαλοποιηθεί, ο κτηνίατρος μπορεί να αποφασίσει να τιτλοποιήσει ή να μην τιτλοποιήσει τη δόση, λαμβάνοντας υπόψη την ανταπόκριση/ανεκτικότητα του ατόμου στη δόση.
Σε περίπτωση που τα κλινικά συμπτώματα δεν ελέγχονται επαρκώς (κλινική αξιολόγηση ή/και διαγνωστικές εξετάσεις) συνιστάται η αύξηση της συνολικής ημερήσιας δόσης με προσαυξήσεις των 0,5 mg (εάν το φάρμακο είναι ανεκτό στη συγκεκριμένη δόση) κάθε 4 έως 6 εβδομάδες έως ότου επέλθει σταθεροποίηση. Εάν εμφανιστούν συμπτώματα μη ανεκτικότητας στη δόση, η θεραπεία θα πρέπει να διακοπεί για 2 έως 3 ημέρες και να αρχίσει εκ νέου με το ήμισυ της προηγούμενης δόσης. Η συνολική ημερήσια δόση μπορεί στη συνέχεια να τιτλοποιηθεί μέχρι το επιθυμητό κλινικό αποτέλεσμα με προσαυξήσεις των 0,5 mg κάθε 2 έως 4 εβδομάδες. Εάν παραλειφθεί μια δόση, η επόμενη προγραμματισμένη δόση θα πρέπει να χορηγηθεί όπως έχει καθορισθεί.
Μετά τη σταθεροποίηση, θα πρέπει να πραγματοποιείται τακτική κλινική αξιολόγηση και διαγνωστικές εξετάσεις κάθε 6 μήνες για την παρακολούθηση της θεραπείας και της δόσης. Όταν δεν υπάρχει εμφανής ανταπόκριση στη θεραπεία, η διάγνωση πρέπει να επανεκτιμάται.
Συμπτώματα υπερδοσολογίας
Δεν υπάρχουν διαθέσιμες πληροφορίες.
Χρόνοι αναμονής
Δεν επιτρέπεται η χρήση σε άλογα τα οποία προορίζονται για ανθρώπινη κατανάλωση.
Τα άλογα που έχουν λάβει θεραπεία δεν μπορούν ποτέ να σφαγιαστούν για ανθρώπινη κατανάλωση.
Το άλογο πρέπει να έχει δηλωθεί ως μη προοριζόμενο για ανθρώπινη κατανάλωση σύμφωνα με την εθνική νομοθεσία περί διαβατηρίων ίππων.
Δεν επιτρέπεται η χρήση σε φοράδες οι οποίες παράγουν γάλα για ανθρώπινη κατανάλωση.
Διάρκεια ζωής
Διάρκεια ζωής του κτηνιατρικού φαρμακευτικού προϊόντος σύμφωνα με τη συσκευασία πώλησης: 30 μήνες.
Ιδιαίτερες προφυλάξεις κατά τη φύλαξη του προϊόντος
Φυλάσσετε στην αρχική συσκευασία για να το προστατεύσετε από το φως.
Φύση και σύνθεση της στοιχειώδους συσκευασίας
Κυψέλες PVC/PE/PVDC-αλουμινίου που περιέχουν 10 δισκία έκαστη.
Κυψέλες OPA/αλουμινίου/PVC-αλουμινίου που περιέχουν 10 δισκία έκαστη.
Χάρτινο κουτί των 10, 30, 60, 90, 100, 120, 160 ή 240 δισκίων.
Μπορεί να μην κυκλοφορούν όλες οι συσκευασίες.
Ιδιαίτερες προφυλάξεις απόρριψης
Τα φάρμακα δεν πρέπει να απορρίπτονται μέσω των λυμάτων ή των οικιακών αποβλήτων. Χρησιμοποιήστε προγράμματα επιστροφής φαρμάκων για την απόρριψη μη χρησιμοποιηθέντων κτηνιατρικών φαρμακευτικών προϊόντων ή άλλων υλικών που προέρχονται από τη χρήση τους σύμφωνα με τις τοπικές απαιτήσεις και με τυχόν εθνικά συστήματα συλλογής που ισχύουν για τα σχετικά κτηνιατρικά φαρμακευτικά προϊόντα.